بیماری کاردیومیوپاتی هیپرتروفیک (Hypertrophic Cardiomyopathy – HCM)

- کاردیومیوپاتی هیپرتروفیک (HCM): وقتی قلب بیش از حد قوی میشود
- پیشگیری از کاردیومیوپاتی هیپرتروفیک
- روشهای درمان کاردیومیوپاتی هیپرتروفیک
- نحوه تشخیص کاردیومیوپاتی هیپرتروفیک
- نشانههای بیماری کاردیومیوپاتی هیپرتروفیک
- اسمهای دیگر بیماری کاردیومیوپاتی هیپرتروفیک
- تفاوت بیماری کاردیومیوپاتی هیپرتروفیک در مردان و زنان
- علت ابتلا به کاردیومیوپاتی هیپرتروفیک
- درمان دارویی کاردیومیوپاتی هیپرتروفیک
- درمان خانگی کاردیومیوپاتی هیپرتروفیک
- رژیم غذایی مناسب برای کاردیومیوپاتی هیپرتروفیک
- عوارض و خطرات کاردیومیوپاتی هیپرتروفیک
- کاردیومیوپاتی هیپرتروفیک در کودکان و دوران بارداری
- طول درمان کاردیومیوپاتی هیپرتروفیک چقدر است
- تفاوت قلب ورزشکار و کاردیومیوپاتی هیپرتروفیک
کاردیومیوپاتی هیپرتروفیک (HCM): وقتی قلب بیش از حد قوی میشود
پیشگیری از کاردیومیوپاتی هیپرتروفیک
صحبت در مورد پیشگیری از کاردیومیوپاتی هیپرتروفیک (Hypertrophic Cardiomyopathy) کمی پیچیده است، زیرا این بیماری در اکثر موارد ریشه ژنتیکی و ارثی دارد. وقتی بیماری در کد ژنتیکی فرد نوشته شده باشد، نمیتوان با رژیم غذایی یا ورزش جلوی بروز تغییرات سلولی اولیه را به طور کامل گرفت. با این حال، مفهوم “پیشگیری” در اینجا معنای متفاوتی پیدا میکند: پیشگیری از مرگ ناگهانی قلبی و پیشگیری از بروز علائم شدید. اگر فردی در خانواده سابقه این بیماری را دارد، مهمترین اقدام پیشگیرانه، انجام آزمایشهای غربالگری ژنتیک و اکوکاردیوگرافی برای تمام اعضای درجه یک خانواده (والدین، خواهر، برادر و فرزندان) است. تشخیص زودهنگام، کلید طلایی پیشگیری از فاجعه است.
در واقع، ما نمیتوانیم جلوی ضخیم شدن عضله قلب را که توسط ژنها دیکته شده بگیریم، اما میتوانیم از عوارض آن جلوگیری کنیم. برای افرادی که ژن این بیماری را دارند اما هنوز علائم واضحی ندارند (فنوتیپ منفی)، تغییرات سبک زندگی میتواند حیاتی باشد. دوری از ورزشهای رقابتی سنگین و حرفهای یکی از این موارد است. ورزشهای استقامتی شدید باعث میشود قلب برای پمپاژ خون فشار زیادی را تحمل کند و این فشار مکانیکی ممکن است باعث تسریع روند ضخیم شدن دیوارهها و یا تحریک آریتمیهای خطرناک شود. بنابراین، شناسایی افراد در معرض خطر قبل از اینکه در میادین ورزشی دچار ایست قلبی شوند، مهمترین استراتژی پیشگیری در سطح جامعه است.
جنبه دیگر پیشگیری، جلوگیری از انتقال ژن به نسل بعد است. با پیشرفتهای علم ژنتیک، زوجهایی که میدانند ناقل ژنهای عامل HCM هستند، میتوانند از روشهای کمک باروری مانند تشخیص ژنتیکی پیش از لانهگزینی (PGD) استفاده کنند. در این روش، جنینها در محیط آزمایشگاه تشکیل شده و تنها جنینهایی که فاقد ژن معیوب هستند به رحم مادر منتقل میشوند. این روش در حال حاضر تنها راه قطعی برای “پیشگیری اولیه” و متوقف کردن چرخه انتقال بیماری در یک خاندان است. همچنین، کنترل دقیق فشار خون در افراد مبتلا بسیار مهم است، زیرا فشار خون بالا خود باعث ضخیم شدن قلب میشود و اگر با HCM همراه شود، وضعیت را بسیار وخیمتر میکند.
روشهای درمان کاردیومیوپاتی هیپرتروفیک
درمان کاردیومیوپاتی هیپرتروفیک بر اساس شدت علائم و میزان خطر مرگ ناگهانی برای هر بیمار شخصیسازی میشود. هدف اصلی درمان، کاهش علائم (مانند تنگی نفس و درد سینه) و پیشگیری از ایست قلبی است. خط اول درمان معمولاً دارویی است که در بخشهای بعد به تفصیل بررسی میشود، اما زمانی که داروها نتوانند علائم را کنترل کنند یا انسداد مسیر خروجی قلب شدید باشد، روشهای تهاجمیتر (Invasive) مطرح میشوند. یکی از استانداردترین روشهای جراحی، میکتومی سپتوم (Septal Myectomy) است. این یک عمل جراحی قلب باز است که در آن جراح بخش کوچکی از عضله ضخیم شده دیواره بین دو بطن را برمیدارد. این کار باعث میشود مسیر خروجی خون از قلب باز شود و انسداد برطرف گردد. این عمل نتایج بسیار درخشانی در بهبود طولانیمدت علائم دارد و اغلب به عنوان “استاندارد طلایی” برای موارد انسدادی مقاوم به دارو شناخته میشود.

روش کمتهاجمیتر دیگری که برای بیمارانی که توانایی تحمل جراحی قلب باز را ندارند استفاده میشود، ابلیشن سپتوم با الکل (Alcohol Septal Ablation) است. در این روش، پزشک از طریق آنژیوگرافی (با استفاده از کاتتر وارد شده از رگ کشاله ران) به شریان تغذیهکننده آن بخش از عضله قلب که ضخیم شده میرسد. سپس مقدار کمی الکل خالص به داخل آن شریان تزریق میشود. الکل باعث میشود سلولهای آن ناحیه خاص دچار نوعی سکته کنترلشده شوند و بمیرند. با گذشت زمان، بافت مرده کوچک و نازک میشود و در نتیجه مسیر خروج خون باز میگردد. اگرچه این روش نیاز به باز کردن قفسه سینه ندارد، اما خطراتی مانند نیاز به ضربانساز (پیسمیکر) دائمی را به همراه دارد.
برای بیمارانی که در معرض خطر بالای مرگ ناگهانی هستند (مثلاً سابقه ایست قلبی نجات یافته دارند یا در خانوادهشان مرگ ناگهانی وجود داشته)، کاشت دستگاه دفیبریلاتور (ICD) حیاتی است. این دستگاه کوچک زیر پوست قفسه سینه قرار میگیرد و سیمهای آن به قلب متصل میشوند. ICD به طور دائم ریتم قلب را پایش میکند و اگر متوجه ریتمهای کشنده مانند فیبریلاسیون بطنی شود، با دادن یک شوک الکتریکی قوی، قلب را به ریتم عادی برمیگرداند و جان بیمار را نجات میدهد. اخیراً داروهای جدیدی مانند مavacamten نیز تایید شدهاند که مستقیماً مکانیسم انقباض پروتئینهای قلب را هدف قرار میدهند و انقلابی در درمان غیرجراحی این بیماری ایجاد کردهاند.
نحوه تشخیص کاردیومیوپاتی هیپرتروفیک
تشخیص HCM اغلب با شنیدن یک صدای غیرطبیعی از قلب (سوفل یا Murmur) در حین معاینه روتین پزشکی آغاز میشود. این صدا ناشی از جریان متلاطم خون در هنگام خروج از قلبِ تنگ شده است. اما ابزار اصلی و قطعی برای تشخیص، اکوکاردیوگرافی (سونوگرافی قلب) است. در اکوکاردیوگرافی، پزشک ضخامت دیوارههای قلب را اندازه میگیرد. در حالت طبیعی ضخامت دیواره کمتر از ۱۲ میلیمتر است، اما در بیماران HCM این ضخامت معمولاً به ۱۵ میلیمتر یا بیشتر میرسد، بدون اینکه علت دیگری مثل فشار خون بالا وجود داشته باشد. اکوکاردیوگرافی همچنین نشان میدهد که آیا انسدادی در مسیر خروجی خون وجود دارد یا خیر (انواع انسدادی در مقابل غیرانسدادی) و همچنین وضعیت دریچه میترال را که در این بیماری اغلب دچار مشکل میشود، بررسی میکند.
نوار قلب (ECG) نیز یکی از اولین تستهاست. نوار قلب در بیش از ۹۰ درصد بیماران مبتلا به HCM غیرطبیعی است، حتی اگر بیمار هیچ علامتی نداشته باشد. تغییرات ولتاژ بالا (نشاندهنده بزرگ شدن قلب) و تغییرات موج T در نوار قلب دیده میشود. گاهی اوقات نوار قلب اولین سرنخ در ورزشکاران جوانی است که برای چکاپ مراجعه میکنند. هولتر مانیتورینگ (نوار قلب ۲۴ یا ۴۸ ساعته) نیز برای بررسی آریتمیهای مخفی که میتوانند خطرناک باشند، انجام میشود.
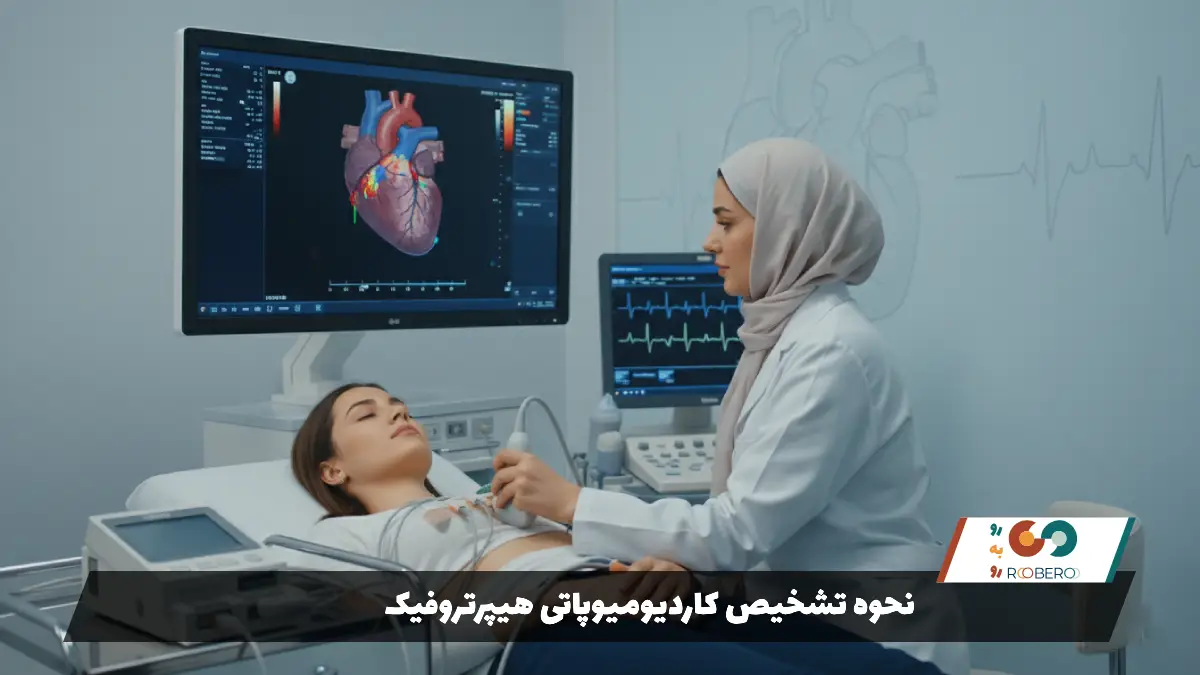
در مواردی که تصاویر اکوکاردیوگرافی واضح نیست یا پزشک نیاز به بررسی دقیقتر بافت قلب (مثلاً برای دیدن میزان فیبروز یا بافت اسکار) دارد، از امآرآی قلب (Cardiac MRI) استفاده میشود. MRI دقیقترین روش برای اندازهگیری ضخامت قلب در تمام نقاط آن است و میتواند انواع خاصی از HCM (مانند نوع آپیکال که نوک قلب را درگیر میکند و در اکو سخت دیده میشود) را به خوبی تشخیص دهد. تست ورزش نیز برای بررسی پاسخ فشار خون به فعالیت و ارزیابی شدت تنگی نفس انجام میشود. در نهایت، آزمایش ژنتیک برای یافتن جهش در ژنهای سازنده پروتئینهای سارکومر (واحدهای انقباضی عضله) انجام میشود که برای تشخیص قطعی در موارد مبهم و همچنین غربالگری خانواده بسیار ارزشمند است.
نشانههای بیماری کاردیومیوپاتی هیپرتروفیک
کاردیومیوپاتی هیپرتروفیک بیماری با “هزار چهره” است؛ برخی بیماران تا پایان عمر طولانی خود هیچ علامتی ندارند، در حالی که برخی دیگر در سنین جوانی دچار علائم شدید میشوند. شایعترین علامت، تنگی نفس (Dyspnea) است، به ویژه در هنگام فعالیت بدنی. علت این تنگی نفس این است که عضله قلب ضخیم شده، “سفت” میشود و نمیتواند به خوبی شل شود تا خون کافی را دریافت کند. در نتیجه، فشار در ریهها بالا میرود و فرد احساس کمبود نفس میکند. این علامت اغلب با آسم اشتباه گرفته میشود، به خصوص در جوانان.
درد قفسه سینه (آنژین) نیز بسیار شایع است و میتواند در هنگام ورزش یا حتی استراحت رخ دهد. این درد به دلیل عدم تعادل بین نیاز عضله قلب ضخیم شده به اکسیژن و توانایی عروق کرونر برای تامین آن ایجاد میشود (ایسکمی). حتی اگر رگهای اصلی قلب باز باشند، عروق ریز داخل بافت قلب ممکن است تحت فشار عضله ضخیم له شوند و نتوانند خونرسانی کنند. تپش قلب (Palpitations) نیز علامت دیگری است که نشاندهنده اختلال در سیستم الکتریکی قلب است و ممکن است ناشی از فیبریلاسیون دهلیزی یا آریتمیهای بطنی باشد.
اما نگرانکنندهترین علامت، سنکوپ (غش کردن) است. اگر فردی (بهویژه یک جوان) در حین ورزش یا فعالیت بدنی ناگهان بیهوش شود، این یک زنگ خطر بسیار جدی برای HCM است. غش کردن میتواند ناشی از انسداد ناگهانی مسیر خروجی قلب یا یک آریتمی خطرناک باشد. سرگیجه و سیاهی رفتن چشمها هنگام برخاستن سریع نیز ممکن است رخ دهد. در تعدادی از بیماران، متاسفانه اولین و آخرین علامت بیماری، مرگ ناگهانی قلبی است؛ به همین دلیل توجه به علائم هشداردهنده و سابقه خانوادگی بسیار حیاتی است. خستگی مفرط و کاهش توانایی انجام فعالیتهای روزمره نیز با پیشرفت بیماری دیده میشود.
اسمهای دیگر بیماری کاردیومیوپاتی هیپرتروفیک
این بیماری در طول تاریخ پزشکی با نامهای بسیار متنوعی شناخته شده است که این تنوع گاهی باعث سردرگمی بیماران میشود. نام رسمی و پذیرفتهشده جهانی HCM (Hypertrophic Cardiomyopathy) است. اما اگر در بیماری، ضخامت عضله باعث مسدود شدن مسیر خروج خون از بطن چپ شود، به آن HOCM (Hypertrophic Obstructive Cardiomyopathy) میگویند. این کلمه “Obstructive” یا انسدادی، کلید تمایز بین دو نوع اصلی بیماری است.
یکی از نامهای قدیمی که هنوز هم در متون قدیمی یا توسط برخی پزشکان مسنتر استفاده میشود، IHSS است که مخفف “Idiopathic Hypertrophic Subaortic Stenosis” (تنگی زیر آئورتی هیپرتروفیک با علت ناشناخته) میباشد. این نام به محل دقیق تنگی (زیر دریچه آئورت) اشاره دارد. نام توصیفی دیگری که به کار میرود، ASH (Asymmetric Septal Hypertrophy) یا “هیپرتروفی نامتقارن سپتوم” است. این نام به ویژگی بارز بیماری اشاره دارد که در آن دیواره بین دو بطن (سپتوم) بسیار بیشتر از سایر دیوارههای قلب ضخیم میشود (برخلاف قلب ورزشکاران یا فشار خون که ضخامت متقارن است).
گاهی نیز ممکن است اصطلاح “Muscular Subaortic Stenosis” یا تنگی عضلانی زیر آئورت را بشنوید. در مواردی که ضخامت فقط در نوک قلب (Apex) باشد، به آن “کاردیومیوپاتی هیپرتروفیک آپیکال” (Apical HCM) یا سندرم یاماگوچی (Yamaguchi Syndrome) میگویند که در نژاد آسیای شرقی شایعتر است. همه این نامها در واقع به یک بیماری واحد با طیفهای مختلفی از تظاهرات آناتومیک اشاره دارند.
تفاوت بیماری کاردیومیوپاتی هیپرتروفیک در مردان و زنان
اگرچه کاردیومیوپاتی هیپرتروفیک یک بیماری ژنتیکی با الگوی وراثت اتوزومال غالب است (یعنی شانس انتقال به دختر و پسر برابر است)، اما در دنیای واقعی، آمار تشخیص در مردان بیشتر از زنان است. تقریباً ۶۰ درصد موارد تشخیص داده شده مرد هستند. علت این تفاوت هنوز کاملاً مشخص نیست، اما ممکن است بخشی از آن به دلیل هورمونهای جنسی باشد که باعث میشوند تظاهر بیماری (ضخامت قلب) در مردان بارزتر باشد یا اینکه زنان دیرتر به پزشک مراجعه میکنند.
مطالعات نشان دادهاند که زنان مبتلا به HCM اغلب در سنین بالاتر تشخیص داده میشوند و متاسفانه در زمان تشخیص، علائم شدیدتر و وضعیت بدتری نسبت به مردان همسن خود دارند. زنان بیشتر از مردان علائمی مانند تنگی نفس شدید و نارسایی قلبی را گزارش میکنند. همچنین احتمال اینکه زنان به عنوان “اشتباه تشخیص” (Misdiagnosis) درمان شوند بیشتر است؛ مثلاً علائم آنها به اشتباه به اضطراب، آسم یا پیری نسبت داده میشود.
از نظر ژنتیکی تفاوتی وجود ندارد، اما از نظر پیامد، برخی تحقیقات نشان میدهند که خطر مرگومیر ناشی از نارسایی قلبی یا سکته مغزی (ناشی از فیبریلاسیون دهلیزی) در زنان مبتلا به HCM ممکن است کمی بیشتر از مردان باشد. این مسئله لزوم توجه ویژه و جدی گرفتن علائم قلبی در زنان را، حتی اگر در نوار قلب تغییرات خفیفی داشته باشند، برجسته میکند. در مقابل، مردان جوان بیشتر در معرض خطر مرگ ناگهانی در حین ورزش هستند، شاید به این دلیل که مردان بیشتر درگیر ورزشهای رقابتی سنگین میشوند.
علت ابتلا به کاردیومیوپاتی هیپرتروفیک
علت اصلی و بنیادین کاردیومیوپاتی هیپرتروفیک، جهشهای ژنتیکی است. قلب ما از میلیاردها سلول عضلانی ساخته شده و درون این سلولها پروتئینهای بسیار ریزی وجود دارند که با لغزیدن روی هم، باعث انقباض قلب میشوند (سارکومر). در بیماران HCM، ژنهایی که دستور ساخت این پروتئینها (مانند میوزین و اکتین) را میدهند، دارای غلط املایی (جهش) هستند. شایعترین ژنهای درگیر MYH7 و MYBPC3 هستند. این جهش باعث میشود پروتئینهای انقباضی قلب “کمبازده” باشند یا انرژی زیادی مصرف کنند.
برای جبران این ناکارآمدی، عضله قلب شروع به ضخیم شدن و بزرگ شدن (هیپرتروفی) میکند تا بتواند کار خود را انجام دهد. علاوه بر ضخیم شدن، چیدمان سلولهای قلبی نیز به هم میریزد. در یک قلب سالم، سلولها مثل آجرچینی منظم کنار هم قرار دارند، اما در HCM، سلولها دچار “درهمریختگی” (Disarray) میشوند و با زوایای نامنظم کنار هم قرار میگیرند. این درهمریختگی زمینه را برای اختلالات الکتریکی و آریتمی فراهم میکند.
وراثت این بیماری به صورت “اتوزومال غالب” است. این یعنی اگر یکی از والدین (پدر یا مادر) مبتلا باشد، به احتمال ۵۰ درصد این ژن به هر یک از فرزندان منتقل میشود. لازم نیست هر دو والدین بیمار باشند. البته در موارد نادری، جهش میتواند به صورت جدید (De novo) در خود فرد ایجاد شود بدون اینکه والدینش بیمار باشند. برخلاف تصور عمومی، این بیماری ناشی از ورزش زیاد یا فشار خون بالا نیست (هرچند فشار خون میتواند آن را تشدید کند)، بلکه یک مشکل ذاتی و ساختاری در معماری سلولهای قلب است.
درمان دارویی کاردیومیوپاتی هیپرتروفیک
دارودرمانی در HCM با هدف کاهش علائم و بهبود عملکرد قلب انجام میشود. دسته اصلی داروها، بتا بلاکرها (Beta-blockers) هستند (مانند متوپرولول، آتنولول، پروپرانولول). این داروها با کند کردن ضربان قلب، زمان بیشتری را به قلب میدهند تا در مرحله استراحت (دیاستول) از خون پر شود. همچنین قدرت انقباض قلب را کمی کاهش میدهند که در موارد انسدادی مفید است، زیرا انقباض کمتر به معنی انسداد کمتر مسیر خروجی است. بتا بلاکرها همچنین درد قفسه سینه را با کاهش نیاز قلب به اکسیژن بهبود میبخشند.
اگر بیمار نتواند بتا بلاکر مصرف کند (مثلاً آسم داشته باشد)، از مسدودکنندههای کانال کلسیم (Calcium Channel Blockers) نوع غیر دیهیدروپیریدینی مانند وراپامیل (Verapamil) یا دیلتیازم استفاده میشود. این داروها نیز اثراتی مشابه بتا بلاکرها دارند و باعث شل شدن عضله قلب و بهبود پر شدن آن میشوند. داروی دیگری به نام دیزوپیرامید (Disopyramide) نیز وجود دارد که قدرت انقباض قلب را کاهش میدهد و به طور خاص برای کاهش انسداد شدید در بیمارانی که با بتا بلاکر خوب نشدهاند، تجویز میشود.
یک پیشرفت انقلابی در درمان دارویی، داروی جدیدی به نام ماواکامتن (Mavacamten) است. این اولین دارویی است که مستقیماً مکانیسم بیماری را هدف قرار میدهد. ماواکامتن با مهار اتصالهای بیشازحد پروتئینهای میوزین و اکتین، باعث میشود عضله قلب بیش از حد منقبض نشود و انسداد برطرف گردد. نکته بسیار مهم در درمان دارویی HCM این است که برخی داروها برای این بیماران ممنوع یا خطرناک هستند. دیورتیکها (ادرارآورها) و گشادکنندههای عروق (مانند نیتروگلیسیرین یا داروهای فشار خون معمولی) باید با احتیاط شدید مصرف شوند، زیرا با کاهش حجم خون، میتوانند انسداد مسیر خروجی را تشدید کرده و باعث غش کردن بیمار شوند.
درمان خانگی کاردیومیوپاتی هیپرتروفیک
درمان خانگی برای بیماران HCM بیشتر بر پایه “مدیریت سبک زندگی” استوار است. مهمترین اصل در خانه، هیدراتاسیون (آبرسانی) کافی است. کمآبی بدن (Dehydration) دشمن شماره یک بیماران مبتلا به نوع انسدادی است. وقتی حجم خون کم شود، فضای داخل بطن چپ کوچک شده و انسداد مسیر خروجی شدیدتر میشود که میتواند منجر به سرگیجه یا غش شود. بنابراین، نوشیدن آب کافی به خصوص در هوای گرم یا هنگام بیماریهای گوارشی بسیار حیاتی است.
اجتناب از فعالیتهای سنگین ناگهانی نیز بخشی از مراقبت خانگی است. بیماران باید یاد بگیرند که “به صدای بدن خود گوش دهند”. اگر در حین انجام کاری (مانند پله بالا رفتن) دچار تنگی نفس یا درد سینه شدند، باید بلافاصله متوقف شوند و استراحت کنند تا ضربان قلب پایین بیاید. بلند کردن اجسام بسیار سنگین (مانند جابجایی مبلمان) که باعث حبس نفس و فشار زیاد (مانور والسالوا) میشود، باید محدود گردد.
مدیریت استرس و اضطراب نیز بسیار کمککننده است، زیرا استرس باعث ترشح آدرنالین میشود که خود انقباض قلب و انسداد را بدتر میکند. تکنیکهای ریلکسیشن و یوگای سبک میتواند مفید باشد. همچنین، محیط خانه باید ایمن باشد تا در صورت بروز سرگیجه یا غش، آسیب فیزیکی کمتری به فرد وارد شود (مثلاً استفاده از کفپوش نرم یا دستگیره در حمام). آموزش احیای قلبی-ریوی (CPR) به اعضای خانواده یک اقدام هوشمندانه خانگی برای آمادگی در شرایط اضطراری است.
رژیم غذایی مناسب برای کاردیومیوپاتی هیپرتروفیک
رژیم غذایی در HCM اصولاً همان رژیم “دوستدار قلب” است، اما با چند تفاوت ظریف نسبت به سایر بیماران قلبی. برخلاف بیماران نارسایی قلبی که باید مصرف آب و نمک را به شدت محدود کنند، بیماران HCM (مگر اینکه وارد فاز نارسایی نهایی شده باشند) معمولاً نیاز به حجم خون کافی دارند؛ بنابراین محدودیت شدید مایعات و نمک ممکن است برای آنها مضر باشد. البته این به معنای مصرف نمک زیاد نیست، بلکه به معنای حفظ تعادل الکترولیتها و مایعات است.
مصرف وعدههای غذایی سنگین و حجیم میتواند باعث تشدید علائم شود. وقتی معده پر است، خون زیادی به سمت دستگاه گوارش میرود و ضربان قلب بالا میرود که میتواند باعث تنگی نفس یا تپش قلب شود. بنابراین توصیه میشود بیماران از وعدههای غذایی کوچکتر و متعددتر استفاده کنند. مصرف الکل باید به شدت محدود یا قطع شود. الکل نه تنها باعث کمآبی بدن میشود، بلکه گشادکننده عروق است (که انسداد را بدتر میکند) و مهمتر از آن، محرک قوی برای شروع فیبریلاسیون دهلیزی است که در این بیماران بسیار شایع و خطرناک است.
کافئین در حد اعتدال معمولاً مشکلی ایجاد نمیکند، اما در برخی بیماران باعث تپش قلب میشود؛ بنابراین هر فرد باید تحمل خود را بسنجد. مصرف میوهها، سبزیجات، غلات کامل و چربیهای سالم (مانند روغن زیتون و ماهی) برای حفظ سلامت کلی عروق و جلوگیری از بیماری عروق کرونر (که وضعیت HCM را پیچیده میکند) ضروری است. حفظ وزن ایدهآل نیز بسیار مهم است، زیرا چاقی بار اضافی قابل توجهی را به قلبی که خود تحت فشار است، تحمیل میکند.
عوارض و خطرات کاردیومیوپاتی هیپرتروفیک
مهمترین و ترسناکترین عارضه HCM، مرگ ناگهانی قلبی (Sudden Cardiac Death) است. این اتفاق اغلب ناشی از یک آریتمی بطنی سریع (فیبریلاسیون بطنی) است که باعث میشود قلب پمپاژ خون را متوقف کند. متأسفانه HCM شایعترین علت مرگ ناگهانی در ورزشکاران جوان زیر ۳۵ سال است. با این حال، باید دانست که این اتفاق در کل جمعیت بیماران نادر است (کمتر از ۱ درصد در سال) و اکثر بیماران عمر طبیعی دارند. شناسایی افراد پرخطر و استفاده از ICD راهکار مقابله با این خطر است.
عارضه شایع دیگر، فیبریلاسیون دهلیزی (AFib) است. حدود ۲۰ تا ۲۵ درصد بیماران HCM در طول زندگی خود دچار این آریتمی میشوند. در این حالت دهلیزها به جای انقباض منظم، میلرزند. این مسئله دو مشکل ایجاد میکند: اول اینکه پر شدن بطن ضخیم و سفت مختل میشود و بیمار دچار تنگی نفس شدید میگردد؛ دوم اینکه خطر تشکیل لخته خون در دهلیز و پرتاب آن به مغز (سکته مغزی) به شدت بالا میرود. به همین دلیل بیماران مبتلا به AFib حتماً باید داروهای رقیقکننده خون (ضد انعقاد) مصرف کنند.
نارسایی قلبی پیشرونده نیز یکی از عوارض درازمدت است. در درصد کمی از بیماران (حدود ۵ تا ۱۰ درصد)، عضله قلب به مرور زمان ضعیف و نازک میشود (فاز Burn-out) و قلب گشاد میگردد که علائمی شبیه به سایر انواع نارسایی قلبی ایجاد میکند. عفونت دریچه قلب (اندوکاردیت) نیز در بیماران مبتلا به نوع انسدادی کمی شایعتر است، زیرا جریان متلاطم خون میتواند به دریچه آسیب زده و آن را مستعد عفونت کند.
کاردیومیوپاتی هیپرتروفیک در کودکان و دوران بارداری
در کودکان، تشخیص HCM میتواند چالشبرانگیز باشد. غربالگری خانواده در سنین پایین توصیه میشود، اما گاهی اوقات ضخیم شدن قلب تا سنین نوجوانی (که جهش رشد رخ میدهد) ظاهر نمیشود. بنابراین یک بار اکوکاردیوگرافی منفی در کودکی به معنای سالم بودن قطعی نیست و باید در دوران بلوغ تکرار شود. کودکان مبتلا به HCM باید از نظر شرکت در ورزشهای مدرسه و کلاسهای تربیت بدنی ارزیابی شوند. معمولاً ورزشهای رقابتی ممنوع میشود، اما فعالیتهای تفریحی سبک تشویق میگردد تا کودک دچار انزوای اجتماعی و چاقی نشود.
دوران بارداری برای زنان مبتلا به HCM معمولاً به خوبی طی میشود، اما نیازمند مراقبتهای ویژه است. در بارداری حجم خون مادر تا ۵۰ درصد افزایش مییابد. برای اکثر زنان مبتلا، این افزایش حجم خون در واقع کمککننده است (چون انسداد را کم میکند)، اما برای کسانی که نارسایی قلبی یا علائم شدید دارند، بار اضافی میتواند مشکلساز شود. داروهایی مانند بتا بلاکرها (مثلاً متوپرولول) در بارداری نسبتاً ایمن هستند و اغلب ادامه مییابند، اما برخی داروها باید قطع شوند.
مهمترین خطر در بارداری و زایمان، نوسانات فشار خون و خونریزی است. زایمان طبیعی (واژینال) برای اکثر این زنان ایمن و حتی ترجیح داده میشود، اما بیحسی نخاعی (اپیدورال) باید با احتیاط فراوان و توسط متخصص بیهوشی آگاه به بیماری انجام شود، زیرا میتواند باعث افت ناگهانی فشار خون و تشدید انسداد قلبی شود. تیم پزشکی باید مراقب باشند تا از کمآبی و درد شدید مادر جلوگیری کنند.
طول درمان کاردیومیوپاتی هیپرتروفیک چقدر است
کاردیومیوپاتی هیپرتروفیک یک بیماری مزمن و مادامالعمر است. هیچ درمانی وجود ندارد که بتواند جهش ژنتیکی را اصلاح کند و بیماری را “ریشهکن” نماید (مگر در آینده با ژندرمانی). بنابراین، “طول درمان” برابر با تمام سالهای باقیمانده عمر بیمار است. بیماران باید بپذیرند که داروهای خود را به طور منظم مصرف کنند و تحت نظر متخصص قلب باقی بمانند.
سیر بیماری در افراد مختلف بسیار متفاوت است. بسیاری از افراد تا سنین پیری بدون مشکل خاصی زندگی میکنند و تنها نیاز به چکاپ سالانه دارند. در برخی دیگر، ممکن است نیاز باشد داروها در طول زمان تغییر کنند یا دوز آنها افزایش یابد. عمل جراحی (میکتومی) معمولاً یک بار انجام میشود و اثرات آن برای دهها سال باقی میماند و بسیاری از بیماران پس از جراحی دیگر نیازی به دارو ندارند یا دوز داروی آنها بسیار کم میشود.
پیگیری مداوم پزشکی بسیار مهم است. معمولاً توصیه میشود بیماران هر ۱۲ تا ۱۸ ماه یکبار اکوکاردیوگرافی و هولتر ریتم قلب انجام دهند تا هرگونه تغییر در ضخامت قلب یا بروز آریتمیهای جدید به سرعت شناسایی شود. با مدیریت صحیح و درمانهای مدرن، امید به زندگی در بیماران HCM امروزه تقریباً برابر با امید به زندگی در جمعیت عمومی است. این بیماری دیگر حکم مرگ ندارد، بلکه شرایطی است که باید با آن زندگی کرد و مدیریتش نمود.
تفاوت قلب ورزشکار و کاردیومیوپاتی هیپرتروفیک
یکی از بزرگترین چالشهای تشخیصی در پزشکی ورزشی، تمایز بین “قلب ورزشکار” (Athlete’s Heart) و HCM خفیف است. ورزشکاران حرفهای که تمرینات سنگین انجام میدهند، به طور فیزیولوژیک قلبشان کمی بزرگ و ضخیم میشود تا بتواند خون بیشتری پمپاژ کند. این یک سازگاری سالم است. ضخامت دیواره قلب در ورزشکاران ممکن است به ۱۳ یا ۱۴ میلیمتر برسد که در محدوده خاکستری تشخیص HCM قرار میگیرد.
تفاوتهای کلیدی وجود دارد: در قلب ورزشکار، ضخامت دیواره متقارن است، اما در HCM معمولاً نامتقارن است (یک طرف ضخیمتر است). در قلب ورزشکار، اندازه حفره بطن چپ نیز بزرگ میشود (قلب گشاد و بزرگ)، اما در HCM حفره بطن اغلب کوچک است. مهمتر از همه، با توقف ورزش (Deconditioning) برای ۳ ماه، ضخامت قلب ورزشکار کاهش مییابد و به حالت عادی برمیگردد، اما در HCM ضخامت ثابت میماند. استفاده از تستهای پیشرفته ژنتیک و MRI به پزشکان کمک میکند تا این دو را از هم افتراق دهند، زیرا تشخیص اشتباه میتواند منجر به محرومیت بیدلیل یک ورزشکار سالم یا مرگ ناگهانی یک ورزشکار بیمار شود.
جمعبندی
کاردیومیوپاتی هیپرتروفیک (HCM) یک بیماری ژنتیکی شایع است که باعث ضخیم شدن غیرطبیعی عضله قلب میشود. این ضخامت میتواند مسیر خروج خون را مسدود کند (نوع انسدادی) یا باعث سفتی قلب شود. اگرچه بسیاری از بیماران بدون علامت هستند، اما علائم کاردیومیوپاتی هیپرتروفیک شامل تنگی نفس، درد سینه، تپش قلب و غش کردن است. مهمترین خطر این بیماری، مرگ ناگهانی قلبی در افراد جوان است، هرچند که احتمال آن کم است و با روشهای درمان مدرن مانند داروها (بتا بلاکرها)، جراحی (میکتومی) و دستگاههای ICD قابل پیشگیری و مدیریت است.
تشخیص قطعی با اکوکاردیوگرافی و تستهای ژنتیک انجام میشود. بیماران باید از کمآبی بدن و ورزشهای سنگین رقابتی پرهیز کنند، اما میتوانند زندگی فعال و طولانی داشته باشند. درمان دارویی و سبک زندگی سالم نقش کلیدی در کنترل بیماری دارد. غربالگری اعضای خانواده برای شناسایی موارد خاموش بیماری حیاتی است. HCM پایان راه نیست، بلکه وضعیتی است که با آگاهی و مراقبت صحیح، میتوان بر آن مسلط شد و زندگی باکیفیتی را تجربه کرد.

