بیماری آنژیومیلوپاتی آمیلوئید مغزی (Cerebral Amyloid Angiopathy – CAA)
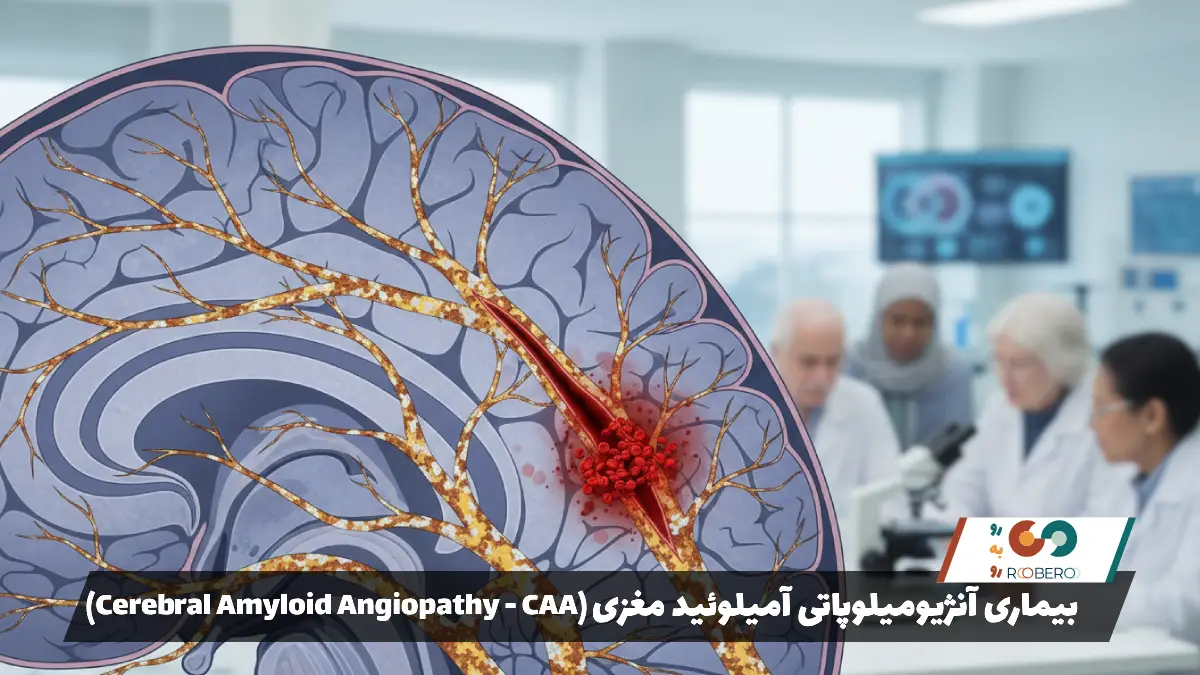
- بیماری آنژیومیلوپاتی آمیلوئید مغزی (Cerebral Amyloid Angiopathy)
- اسم های دیگر بیماری آنژیوپاتی آمیلوئید مغزی
- علت ابتلا به آنژیوپاتی آمیلوئید مغزی
- نشانه های بیماری آنژیوپاتی آمیلوئید مغزی
- نحوه تشخیص آنژیوپاتی آمیلوئید مغزی
- عوارض و خطرات آنژیوپاتی آمیلوئید مغزی
- تفاوت بیماری آنژیوپاتی آمیلوئید مغزی در مردان و زنان
- آنژیوپاتی آمیلوئید مغزی در کودکان و در دوران بارداری
- روش های درمان آنژیوپاتی آمیلوئید مغزی
- درمان دارویی آنژیوپاتی آمیلوئید مغزی
- طول درمان آنژیوپاتی آمیلوئید مغزی چقدر است
- پیشگیری از آنژیوپاتی آمیلوئید مغزی
- درمان خانگی آنژیوپاتی آمیلوئید مغزی
- رژیم غذایی مناسب برای آنژیوپاتی آمیلوئید مغزی
- ارتباط آنژیوپاتی آمیلوئید مغزی با بیماری آلزایمر
بیماری آنژیومیلوپاتی آمیلوئید مغزی (Cerebral Amyloid Angiopathy)
مغز انسان اندامی فوقالعاده پیچیده و نیازمند مراقبت مداوم است. این اندام حیاتی برای عملکرد صحیح به شبکهای گسترده از رگهای خونی نیاز دارد تا اکسیژن و مواد مغذی را به تکتک سلولهای عصبی برساند. بیماری آنژیومیلوپاتی آمیلوئید مغزی که در متون پزشکی معتبر بیشتر با نام آنژیوپاتی آمیلوئید مغزی شناخته میشود، یک اختلال پیشرونده و مرتبط با افزایش سن است که دقیقا همین شبکه حیاتی خونرسانی را هدف قرار میدهد. در این بیماری، یک نوع پروتئین خاص به نام آمیلوئید به مرور زمان در دیواره رگهای خونی کوچک و متوسط مغز رسوب میکند. برای درک بهتر، میتوانید رگهای مغز را مانند لولههای انتقال آب در نظر بگیرید و پروتئین آمیلوئید را مانند رسوبات و زنگزدگیهایی که در طول سالها روی دیواره داخلی این لولهها مینشینند.
با گذشت زمان، تجمع این رسوبات پروتئینی باعث میشود که دیواره رگهای خونی ضخیم، سفت و در عین حال به شدت شکننده و آسیبپذیر شود. این شکنندگی فوقالعاده خطرناک است زیرا رگهای خونی مغز باید بتوانند در برابر نوسانات طبیعی فشار خون مقاومت کنند، اما رگهای درگیر در این بیماری خاصیت ارتجاعی خود را از دست دادهاند. در نتیجه، این رگها مستعد پاره شدن و ایجاد خونریزی در بافت مغز میشوند. این خونریزیها میتوانند به صورت نشتهای بسیار ریز و میکروسکوپی (میکروبلید) باشند که شاید در ابتدا علائم واضحی ایجاد نکنند، یا به صورت خونریزیهای بزرگ و ناگهانی بروز کنند که یک اورژانس پزشکی تمامعیار محسوب میشود و میتواند جان بیمار را به خطر بیندازد یا منجر به آسیبهای عصبی دائمی شود.
این بیماری یکی از دلایل اصلی خونریزیهای مغزی در افراد سالمند است و متاسفانه به دلیل ماهیت خاموش خود، معمولا تا زمانی که یک خونریزی جدی رخ ندهد یا بیمار دچار زوال عقل نشود، تشخیص داده نمیشود. درک این بیماری، مکانیزم اثر آن بر رگهای مغز و چالشهایی که برای سلامت روان و جسم ایجاد میکند، برای بیماران و خانوادههایشان بسیار مهم است. در ادامه این مقاله، به صورت جامع و با زبانی ساده و علمی، تمام ابعاد این اختلال عروقی و عصبی را بررسی خواهیم کرد تا تصویری روشن از نحوه مدیریت و رویارویی با آن به دست آورید.
اسم های دیگر بیماری آنژیوپاتی آمیلوئید مغزی
در دنیای پزشکی، نامگذاری بیماریها معمولا بر اساس مکانیزم سلولی، محل درگیری یا دانشمندانی که اولین بار آنها را کشف کردهاند، انجام میشود. بیماری آنژیوپاتی آمیلوئید مغزی نیز در مقالات علمی، گزارشهای رادیولوژی و پروندههای بیمارستانی ممکن است با عبارات و اصطلاحات متفاوتی نوشته شود. آگاهی از این نامهای جایگزین به شما کمک میکند تا هنگام مطالعه برگه آزمایش یا صحبت با متخصصان مغز و اعصاب دچار سردرگمی نشوید.
یکی از شناختهشدهترین نامهای جایگزین برای این بیماری، “آنژیوپاتی کونگوفیلیک” است. این نام ریشه در روشهای آزمایشگاهی دارد. وقتی پاتولوژیستها میخواهند وجود رسوبات آمیلوئید را در نمونه بافت مغز زیر میکروسکوپ بررسی کنند، از یک رنگ شیمیایی خاص به نام “قرمز کونگو” (Congo Red) استفاده میکنند. پروتئینهای آمیلوئید این رنگ را به خود جذب کرده و زیر نور مخصوص درخشش خاصی پیدا میکنند. به همین دلیل، در متون پزشکی قدیمیتر و گزارشهای پاتولوژی، به رگهایی که این پروتئین در آنها رسوب کرده، رگهای کونگوفیلیک میگویند و کل بیماری با این نام شناخته میشود.
علاوه بر این، گاهی اوقات پزشکان در گزارشهای تصویربرداری از اصطلاحاتی مانند “میکروبلیدینگهای مرتبط با آمیلوئید” یا “خونریزیهای لوبار سالمندان” استفاده میکنند. اگرچه این اصطلاحات مستقیما نام بیماری نیستند، اما توصیفکننده بارزترین نشانههای آن در اسکن مغزی هستند. خونریزی لوبار به خونریزیهایی گفته میشود که در بخشهای بیرونی و قشری مغز (لوبها) رخ میدهد، جایی که رگهای درگیر در این بیماری بیشتر قرار دارند. بنابراین، اگر در پرونده پزشکی یک فرد سالمند با عباراتی نظیر رسوب آمیلوئید عروقی، آنژیوپاتی کونگوفیلیک یا خونریزیهای مکرر لوبار مواجه شدید، همگی به یک روند فرسایشی مشترک در رگهای مغز اشاره دارند.
علت ابتلا به آنژیوپاتی آمیلوئید مغزی
علت بنیادین و اصلی ابتلا به این بیماری، تجمع غیرطبیعی و تدریجی یک نوع پروتئین به نام بتا-آمیلوئید در دیواره رگهای خونی مغز است. اما چرا این اتفاق میافتد؟ در یک مغز سالم و جوان، سلولهای عصبی به طور مداوم فعالیت میکنند و در نتیجه این فعالیتها، مواد زائدی از جمله قطعات پروتئینی تولید میشوند. بدن انسان دارای سیستمهای پاکسازی بسیار دقیقی است که این مواد زائد را از بافت مغز جمعآوری کرده و از طریق جریان خون دفع میکنند. بتا-آمیلوئید نیز یکی از همین پروتئینهاست که در حالت طبیعی باید از مغز خارج شود.
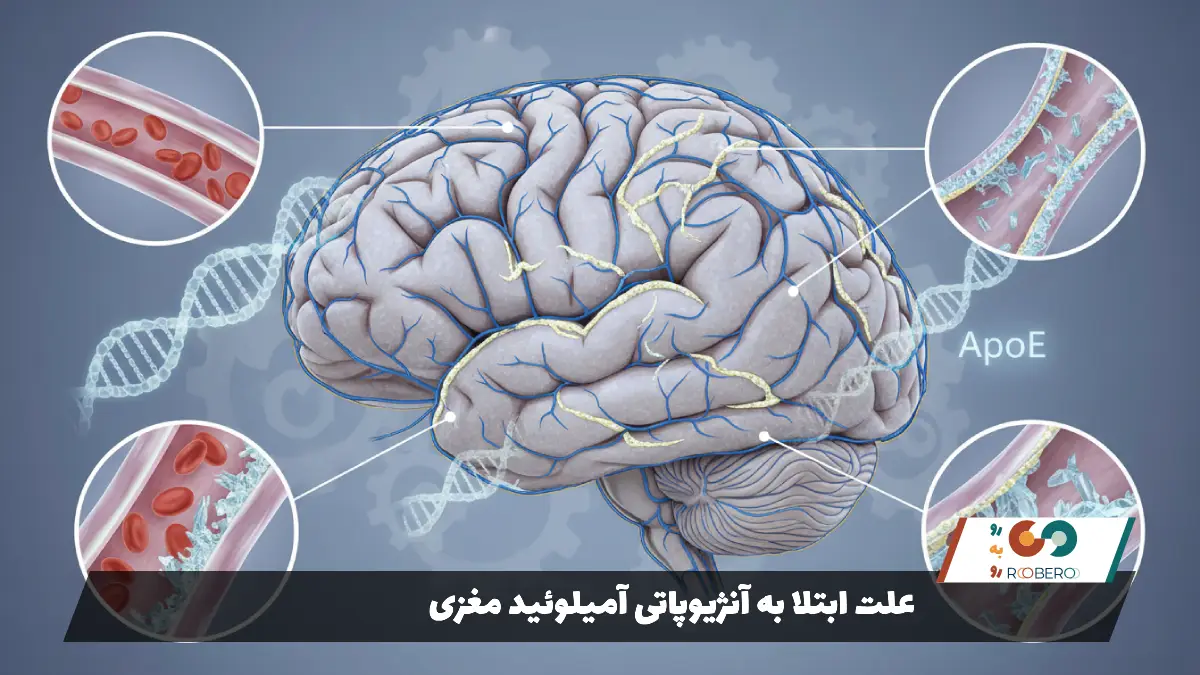
با افزایش سن، در برخی افراد این سیستم پاکسازی و تخلیه مواد زائد دچار اختلال میشود. پروتئینهای بتا-آمیلوئید به جای اینکه به درستی از بافت مغز و رگها دفع شوند، در دیواره رگهای خونی کوچک و متوسط (به ویژه رگهای موجود در پردههای پوشاننده مغز و قشر خارجی آن) گیر میافتند و رسوب میکنند. تجمع این پروتئینها باعث جایگزینی سلولهای عضلانی سالم در دیواره رگ با مواد آمیلوئیدی میشود. این فرآیند جایگزینی، رگ را از یک لوله انعطافپذیر و زنده، به یک لوله خشک، شکننده و مرده تبدیل میکند که توانایی انقباض و انبساط طبیعی خود را از دست داده است.
دلیل اینکه چرا سیستم پاکسازی مغز در برخی افراد از کار میافتد هنوز به طور کامل کشف نشده است، اما علم ژنتیک نقش پررنگی در آن دارد. وجود ژنهای خاصی مانند آپولیپوپروتئین ای (ApoE) به شدت با افزایش خطر رسوب این پروتئینها در رگهای مغز مرتبط است. به غیر از موارد نادر ژنتیکی که در سنین جوانی بروز میکنند، عامل اصلی و غیرقابل تغییر در بروز این بیماری، پدیده پیری و افزایش سن است. هرچه سن فرد بالاتر میرود، احتمال تجمع این پروتئینهای مخرب در رگهای مغز به صورت تصاعدی افزایش مییابد، به طوری که در افراد بالای هشتاد سال، وجود مقادیری از این رسوبات در مغز بسیار شایع است.
نشانه های بیماری آنژیوپاتی آمیلوئید مغزی
یکی از چالشبرانگیزترین جنبههای این بیماری عروقی، خاموش بودن آن در مراحل اولیه است. رسوب پروتئینها در دیواره رگها فرآیندی است که دههها طول میکشد و بیمار در این مدت معمولا هیچگونه علامتی احساس نمیکند. نشانههای بیماری معمولا زمانی آشکار میشوند که آسیب به رگها به حدی رسیده باشد که منجر به نشت خون یا انسداد مسیر خونرسانی گردد. این نشانهها طیف وسیعی از علائم گذرا تا حوادث مغزی مرگبار را شامل میشوند.
شایعترین و در عین حال خطرناکترین نشانه این بیماری، بروز خونریزیهای مغزی است که در اصطلاح پزشکی به آن خونریزی لوبار میگویند. برخلاف خونریزیهای ناشی از فشار خون بالا که معمولا در نواحی عمیق مغز رخ میدهند، خونریزیهای این بیماری در نواحی سطحی و نزدیک به قشر مغز اتفاق میافتند. علائم این خونریزی ناگهانی شامل سردرد بسیار شدید و بیسابقه، تهوع و استفراغ، ضعف یا بیحسی ناگهانی در یک طرف بدن، مشکل در صحبت کردن، تغییرات بینایی و در موارد شدید، از دست دادن هوشیاری و کما است. شدت علائم مستقیما به اندازه رگ پاره شده و وسعت خونریزی در بافت مغز بستگی دارد.
علامت مهم دیگری که گاهی قبل از یک خونریزی بزرگ رخ میدهد و به نوعی زنگ خطر بیماری است، حملات عصبی گذرا نام دارد. بیمار ممکن است به صورت ناگهانی احساس سوزنسوزن شدن یا ضعف در دست و پا کند که در عرض چند دقیقه پخش میشود و سپس کاملا برطرف میگردد. این حالت به دلیل نشتهای بسیار ریز خون روی سطح مغز و تحریک سلولهای عصبی ایجاد میشود. علاوه بر خونریزی، از آنجا که رگهای آسیبدیده نمیتوانند خون و اکسیژن کافی را به بافت مغز برسانند، بیماران به تدریج دچار علائم زوال عقل، کاهش حافظه کوتاهمدت، اختلال در تصمیمگیری و تغییرات شخصیتی میشوند که شباهت زیادی به بیماری آلزایمر دارد.
نحوه تشخیص آنژیوپاتی آمیلوئید مغزی
تشخیص قطعی و صددرصدی رسوب پروتئین در رگهای مغز تنها با بررسی بافت مغز زیر میکروسکوپ (پس از نمونهبرداری جراحی یا کالبدشکافی) امکانپذیر است. اما از آنجا که نمونهبرداری از بافت مغز یک روش به شدت تهاجمی و خطرناک است، پزشکان در محیط بالینی برای تشخیص این بیماری از ترکیبی از علائم بیمار، تاریخچه پزشکی و تصویربرداریهای پیشرفته مغزی استفاده میکنند که به آنها معیارهای بوستون (Boston Criteria) گفته میشود.
ابزار اصلی و خط مقدم تشخیص در این بیماری، استفاده از دستگاه امآرآی (MRI) با تکنیکهای تصویربرداری خاص است. تکنیکهایی مانند تصویربرداری حساسیتپذیر (SWI) یا گرادیان اکو (GRE) میتوانند ذرات بسیار ریز آهن را که از نشتهای قدیمی خون (میکروبلیدها) در بافت مغز باقی ماندهاند، به وضوح نشان دهند. اگر پزشک متخصص مغز و اعصاب در اسکن امآرآی یک فرد سالمند، خونریزیهای ریز متعددی را در نواحی بیرونی و قشری مغز مشاهده کند (بدون اینکه نشانهای از آسیب در نواحی عمیق مغز باشد)، این یک نشانه رادیولوژیک بسیار قوی برای وجود این بیماری است.
در مواقع اورژانسی که بیمار با علائم خونریزی شدید مراجعه میکند، اولین اقدام انجام سیتی اسکن (CT Scan) بدون تزریق است. سیتی اسکن میتواند خونریزی حاد و تازه را به سرعت نشان دهد و به پزشک کمک کند تا محل دقیق و وسعت آسیب را ارزیابی نماید. آزمایش مایع مغزینخاعی و اسکنهای پیشرفتهتری مانند اسکن پت (PET Scan) که برای ردیابی پروتئین آمیلوئید استفاده میشوند، در محیطهای تحقیقاتی کاربرد بیشتری دارند. در نهایت، تشخیص “احتمالی” بیماری زمانی توسط پزشک در پرونده ثبت میشود که اسکنها خونریزیهای مشخص لوبار را نشان دهند، سن بیمار بالای ۵۵ سال باشد و علت دیگری مانند تومور، ضربه به سر یا مصرف زیاد داروهای رقیقکننده خون برای توجیه این خونریزیها وجود نداشته باشد.
عوارض و خطرات آنژیوپاتی آمیلوئید مغزی
هنگامی که رگهای خونی مغز در اثر تجمع پروتئینهای مخرب ضعیف و شکننده میشوند، بیمار در معرض زنجیرهای از خطرات و عوارض جبرانناپذیر قرار میگیرد. این بیماری یک روند پیشرونده دارد و آسیبهایی که به مرور زمان به بافت ظریف مغز وارد میکند، میتواند استقلال فردی بیمار را به طور کامل از بین برده و نیازمند مراقبتهای ۲۴ ساعته نماید. بزرگترین تهدید برای جان بیمار، وقوع یک سکته مغزی خونریزیدهنده وسیع است.
هنگامی که یک خونریزی بزرگ در قشر مغز رخ میدهد، خون نشت کرده فشار فیزیکی شدیدی به سلولهای عصبی مجاور وارد کرده و آنها را از بین میبرد. این مرگ سلولی باعث عوارض حرکتی و حسی ماندگار میشود. بسته به اینکه کدام لوب مغز آسیب دیده باشد، بیمار ممکن است توانایی راه رفتن، استفاده از دستها، تکلم صحیح (آفازی) و یا حتی بلع غذا را برای همیشه از دست بدهد. علاوه بر آسیب فیزیکی، خونریزی در سطح مغز میتواند باعث تحریک دائمی قشر مغز شده و بیمار را مستعد ابتلا به بیماری صرع و تشنجهای مکرر در سالهای بعد از خونریزی کند.
از دیگر عوارض بسیار شایع و خاموش این بیماری، زوال عقل عروقی است. حتی اگر بیمار دچار یک خونریزی بزرگ و فلجکننده نشود، خونریزیهای میکروسکوپی متعدد و همچنین نرسیدن اکسیژن کافی به دلیل تنگ شدن رگهای رسوبدار، باعث مرگ تدریجی سلولهای عصبی میشود. بیمار توانایی تمرکز، حل مسئله و یادآوری خاطرات را از دست میدهد. این افت شناختی معمولا سیری پیشرونده دارد و در نهایت باعث میشود بیمار نتواند کارهای ساده روزمره مانند لباس پوشیدن یا مدیریت مالی خود را انجام دهد. همچنین اضطراب، افسردگی و توهم از عوارض روانی هستند که در پی تخریب بافت مغز در این بیماران مشاهده میشوند.
تفاوت بیماری آنژیوپاتی آمیلوئید مغزی در مردان و زنان
در بررسی آماری و اپیدمیولوژی بسیاری از بیماریها، جنسیت نقش تعیینکنندهای در میزان ابتلا دارد. اما وقتی صحبت از ضعیف شدن رگهای مغز در اثر رسوب آمیلوئید به میان میآید، تحقیقات گسترده پزشکی نشان میدهد که این بیماری به طور کلی تفاوت فاحش و معناداری بین مردان و زنان قائل نیست. مهمترین و قدرتمندترین عامل خطر برای این بیماری، افزایش سن است و هر دو جنس با ورود به دهههای هفتاد و هشتاد زندگی، به یک اندازه در معرض خطر انباشت این پروتئینهای فرسایشی قرار میگیرند.
با این حال، برخی از مطالعات ظرافتهای خاصی را در نحوه بروز علائم و پیامدهای بیماری بین زنان و مردان نشان دادهاند. به عنوان مثال، از آنجا که امید به زندگی در زنان به طور متوسط بالاتر از مردان است و زنان معمولا بیشتر عمر میکنند، تعداد مطلق بیماران زن مبتلا به مراحل پیشرفته این بیماری و زوال عقل ناشی از آن، در برخی جوامع بیشتر دیده میشود. مغز زنان سالمند ممکن است به دلیل تغییرات هورمونی پس از یائسگی و کاهش سطح استروژن (که نقش محافظتی برای رگهای خونی دارد)، در برابر آسیبهای ناشی از کمبود اکسیژن و نشت خون آسیبپذیرتر باشد.
از سوی دیگر، مردان به دلیل شیوع بیشتر عوامل خطر ثانویه مانند فشار خون بالای کنترلنشده، مصرف دخانیات و بیماریهای قلبی در سنین میانسالی، ممکن است در صورت ابتلا به این ضعف عروقی، با شدت بیشتری دچار خونریزیهای مرگبار شوند. ترکیب رگهای شکننده آمیلوئیدی با فشار خون بالا در مردان، مانند یک بمب ساعتی عمل میکند. همچنین برخی پژوهشهای ژنتیکی نشان دادهاند که حضور ژن آپولیپوپروتئین (که عامل خطر بیماری است) ممکن است در زنان و مردان الگوهای تخریبی متفاوتی در بافت مغز ایجاد کند. در نهایت، هم زنان و هم مردان سالمند باید با یک چشم به خطرات این بیماری نگاه کرده و مراقبتهای پیشگیرانه را به یک اندازه جدی بگیرند.
آنژیوپاتی آمیلوئید مغزی در کودکان و در دوران بارداری
بروز این بیماری در سنین کودکی، نوجوانی و جوانی (از جمله زنان در سنین بارداری) به قدری نادر است که در متون پزشکی به عنوان موارد استثنایی و بسیار خاص طبقهبندی میشود. همانطور که پیشتر اشاره شد، مکانیزم اصلی این بیماری بر پایه تجمع کند و چند دههای پروتئینهای زائد در رگها استوار است. بنابراین، یک مغز جوان و در حال رشد در حالت طبیعی هرگز دچار چنین فرسایشی نمیشود. اگر یک کودک یا یک فرد جوان دچار این مشکل عروقی شود، علت آن قطعا یک جهش ژنتیکی بسیار نادر و ارثی است.
این جهشهای ژنتیکی خاص (مانند نوع هلندی، ایسلندی یا فلاندری بیماری) باعث میشوند که بدن از همان سالهای اولیه زندگی، پروتئینهای آمیلوئید را به شکل کاملا معیوب و با سرعت بسیار بالا تولید کند و سیستم پاکسازی مغز نیز توانایی دفع آنها را نداشته باشد. در این بیماران خاص، علائم خونریزی مغزی و زوال عقل ممکن است به جای هشتاد سالگی، در دهههای بیست، سی یا چهل زندگی ظاهر شود. برای کودکان حامل این ژنها، مداخلات پزشکی بیشتر در حوزه تحقیقات ژنتیکی و مشاوره خانواده قرار دارد و در حال حاضر راهی برای توقف این روند ژنتیکی وجود ندارد.
در مورد دوران بارداری، اگر یک زن جوان به صورت بسیار نادر دارای یکی از این فرمهای ژنتیکی بیماری باشد، بارداری میتواند برای او یک چالش پزشکی عظیم و پرخطر باشد. بارداری به طور طبیعی با افزایش حجم خون و تغییرات چشمگیر در وضعیت قلب و عروق همراه است. نوسانات فشار خون در دوران بارداری و به ویژه فشارهای فیزیکی شدید هنگام زایمان طبیعی، میتواند رگهای مغزی را که از قبل توسط آمیلوئید ضعیف شدهاند، به نقطه پارگی رسانده و منجر به خونریزی مغزی مرگبار برای مادر شود. در چنین موارد نادری، بیمار باید تحت نظر دقیق تیمی از متخصصان مغز و اعصاب و متخصصان حاملگی پرخطر قرار گیرد و قطعا زایمان به روش سزارین برنامهریزیشده توصیه میشود تا فشار داخل جمجمه به حداقل برسد.
روش های درمان آنژیوپاتی آمیلوئید مغزی
هنگامی که صحبت از درمان این بیماری به میان میآید، باید با یک واقعیت تلخ پزشکی روبرو شویم: در حال حاضر هیچ درمان قطعی، جراحی یا دارویی وجود ندارد که بتواند پروتئینهای آمیلوئید رسوب کرده را از دیواره رگهای مغز پاک کند یا رگهای آسیبدیده و شکننده را به حالت جوان و انعطافپذیر خود بازگرداند. بنابراین، استراتژی درمان توسط متخصصان مغز و اعصاب کاملا بر مبنای “مدیریت بیماری، پیشگیری از خونریزیهای جدید و بهبود کیفیت زندگی بیمار” پایهگذاری میشود.
مهمترین و حیاتیترین روش درمانی در این بیماران، کنترل وسواسی و بسیار دقیق فشار خون است. فشار خون بالا دشمن شماره یک رگهای شکننده آمیلوئیدی است. حتی نوسانات کوچک فشار خون میتواند باعث پاره شدن این رگهای ضعیف شود. پزشکان با تجویز داروهای مناسب تلاش میکنند تا فشار خون بیمار را به صورت مداوم در محدوده کاملا طبیعی و بیخطر نگه دارند. اقدام درمانی بسیار مهم دیگر، بازنگری کامل در لیست داروهای مصرفی بیمار است. بسیاری از سالمندان به دلیل مشکلات قلبی از داروهای ضد پلاکت (مانند آسپرین) یا رقیقکننده خون (مانند وارفارین) استفاده میکنند. در بیماران مبتلا به این ضعف عروقی، مصرف این داروها به شدت خطرناک است و میتواند یک خونریزی ریز را به یک فاجعه بزرگ و کشنده تبدیل کند. پزشک باید خطرات قطع داروی قلبی را در برابر خطر خونریزی مغزی سنجیده و معمولا مصرف این داروها را متوقف میکند.
اگر بیمار دچار خونریزی حاد و بزرگ شده باشد، درمان در محیط اورژانس و بخش مراقبتهای ویژه (ICU) انجام میشود. در این شرایط ممکن است جراح مغز و اعصاب برای کاهش فشار داخل جمجمه و خارج کردن لخته خون بزرگ، عمل جراحی اورژانسی انجام دهد. اما جراحی در این بیماران بسیار پرخطر است، زیرا بافت مغز و رگهای اطراف لخته نیز شکننده هستند و ممکن است در حین عمل دوباره خونریزی کنند. توانبخشی عصبی، فیزیوتراپی، کاردرمانی و گفتاردرمانی بخشهای جداییناپذیر درمان پس از ترخیص از بیمارستان هستند که به مغز کمک میکنند تا عملکردهای از دست رفته را تا حدودی بازیابی کرده و بیمار بتواند با وجود آسیبهای وارد شده، حداکثر استقلال ممکن را در زندگی روزمره داشته باشد.
درمان دارویی آنژیوپاتی آمیلوئید مغزی
درمان دارویی در این بیماران با هدف محافظت از بافت مغز در برابر نوسانات فیزیولوژیک و کنترل علائم آزاردهنده انجام میشود. از آنجا که دارویی برای حل کردن رسوبات پروتئینی وجود ندارد، داروها بیشتر نقش یک سپر دفاعی را بازی میکنند. ستون فقرات درمان دارویی، استفاده از داروهای کاهنده فشار خون است. مهارکنندههای آنزیم مبدل آنژیوتانسین (ACE inhibitors)، مسدودکنندههای گیرنده آنژیوتانسین (ARBs) و مسدودکنندههای کانال کلسیم از جمله داروهای رایجی هستند که برای تنظیم جریان و فشار خون در رگهای آسیبپذیر مغز تجویز میشوند. ثابت نگه داشتن فشار خون با این داروها، اثبات شدهترین روش برای جلوگیری از تکرار خونریزیهاست.
چالش بزرگ دارویی در این بیماری، مدیریت داروهای رقیقکننده خون است. اگر بیماری به دلیل آریتمی قلبی نیاز مبرم به رقیقکننده خون داشته باشد و همزمان اسکن مغز او نشاندهنده رگهای آمیلوئیدی پرخطر باشد، پزشک با یک معمای پیچیده روبرو میشود. در اکثر مواقع، دستور به قطع مصرف داروهایی مانند آسپرین، پلاویکس یا وارفارین داده میشود، زیرا خطر خونریزی کشنده مغزی معمولا بسیار بالاتر از خطر لخته شدن خون در قلب در نظر گرفته میشود. این تصمیمگیری تنها بر عهده یک تیم پزشکی متشکل از متخصص قلب و متخصص مغز و اعصاب است و بیمار هرگز نباید خودسرانه داروهایش را تغییر دهد.
علاوه بر این، پزشک برای مدیریت عوارض ثانویه بیماری نیز دارو تجویز میکند. اگر بیمار به دلیل آسیبهای قشر مغز دچار تشنج شود، داروهای ضد صرع مانند لوتیراستام یا سدیم والپروات با دوز مناسب تجویز میگردند تا از فعالیتهای الکتریکی غیرطبیعی مغز جلوگیری کنند. برای بیمارانی که علائم افت شناختی و زوال عقل را نشان میدهند، گاهی اوقات داروهایی که در بیماری آلزایمر استفاده میشوند (مانند مهارکنندههای کولین استراز از جمله دونپزیل) برای کمک به بهبود موقت حافظه و تمرکز تجویز میشوند، هرچند اثربخشی آنها در این بیماری خاص محدود است. مدیریت دارویی اضطراب و افسردگی نیز برای حفظ کیفیت زندگی بیمار سالمند بسیار ضروری است.
طول درمان آنژیوپاتی آمیلوئید مغزی چقدر است
مفهوم “طول درمان” در بیماریهای مزمن و دژنراتیو (فرسایشی) با بیماریهای عفونی متفاوت است. در یک بیماری عفونی، شما با مصرف یک دوره آنتیبیوتیک کاملا بهبود مییابید، اما بیماری آنژیوپاتی آمیلوئید مغزی یک روند غیرقابل بازگشت است. وقتی رسوبات پروتئینی در دیواره رگها جایگیر شدند، تا پایان عمر با بیمار همراه خواهند بود. بنابراین، پاسخ به این سوال که طول درمان چقدر است، یک کلمه است: مادامالعمر. بیمار باید تا آخرین روز زندگی تحت نظر پزشک بوده و توصیههای مراقبتی را رعایت کند.
فرآیند مدیریت این بیماری به چند فاز زمانی تقسیم میشود. فاز حاد بیماری زمانی است که فرد دچار خونریزی مغزی میشود. این فاز شامل بستری در اورژانس و بخش مراقبتهای ویژه است و معمولا بین دو تا چهار هفته به طول میانجامد. در این مدت، تلاش کادر درمان بر روی زنده نگه داشتن بیمار، توقف خونریزی و کاهش تورم مغز متمرکز است. پس از ترخیص از بیمارستان، فاز توانبخشی آغاز میشود. طول دوره توانبخشی (فیزیوتراپی و گفتاردرمانی) بسته به شدت آسیب وارده به مغز میتواند از چند ماه تا چند سال متغیر باشد. برخی بیماران با تلاش مستمر پیشرفتهای قابل توجهی در بازگرداندن حرکات خود میکنند.
فاز نگهداری و پیشگیری که مهمترین بخش زندگی بیمار را تشکیل میدهد، پایانی ندارد. بیمار باید به صورت روزانه داروهای کنترل فشار خون خود را مصرف کند و به طور دورهای (معمولا هر شش ماه یا یک سال) توسط متخصص مغز و اعصاب ویزیت شود تا اسکنهای جدیدی از مغز او گرفته شده و میزان پیشرفت رسوبات یا بروز نشتهای جدید بررسی گردد. پذیرش این واقعیت که این یک همراه همیشگی در دوران سالمندی است، به خانوادهها کمک میکند تا محیط زندگی ایمنی را برای بیمار فراهم کرده و انتظارات واقعبینانهای از روند پیشرفت بیماری داشته باشند.
پیشگیری از آنژیوپاتی آمیلوئید مغزی
پیشگیری از بیماریهایی که ریشه در افزایش سن و کدهای ژنتیکی دارند، یکی از سختترین مباحث در علم پزشکی است. از آنجا که نمیتوان جلوی پیر شدن سلولها را گرفت یا ژنهای معیوب را به راحتی تغییر داد، پیشگیری اولیه (یعنی جلوگیری کامل از رسوب آمیلوئید در رگها) در حال حاضر با دانش امروزی امکانپذیر نیست. با این وجود، متخصصان بر این باورند که داشتن یک سبک زندگی حمایتکننده از سلامت قلب و عروق میتواند سرعت تخریب رگها را به تاخیر انداخته و از بروز عوارض مرگبار آن (پیشگیری ثانویه) جلوگیری کند.
مهمترین اصل در پیشگیری ثانویه، محافظت از سلامت کلی سیستم گردش خون است. هر عاملی که باعث ضعیف شدن رگهای خونی در سنین جوانی و میانسالی شود، میتواند مغز را در برابر رسوبات آمیلوئید در دوران سالمندی آسیبپذیرتر کند. کنترل دقیق فشار خون از سنین جوانی یکی از این اصول است. فشار خون بالا باعث استرس مکانیکی روی دیواره رگها میشود. همچنین کنترل دیابت و قند خون، زیرا قند بالا به طور مستقیم دیواره رگها را تخریب کرده و باعث التهاب میشود که این التهاب میتواند روند پاکسازی پروتئینهای زائد را مختل کند.
ترک کامل سیگار و عدم مصرف الکل از دیگر اقدامات حیاتی هستند. مواد سمی موجود در دود سیگار باعث تنگی عروق و کاهش اکسیژنرسانی به مغز میشوند. علاوه بر این، جلوگیری از ضربات مکرر به سر در پیشگیری از خونریزیها بسیار مهم است. برای افراد سالمندی که در معرض این بیماری هستند یا اسکنهای آنها نشاندهنده شروع رسوبات است، ایمنسازی محیط خانه (مانند جمع کردن فرشهای لغزنده، نصب دستگیره در حمام و استفاده از نور مناسب) برای جلوگیری از زمین خوردن، حیاتیترین نوع پیشگیری است. یک ضربه کوچک به سر در فردی که رگهای شکنندهای دارد، میتواند منجر به یک خونریزی مغزی کشنده شود. حفظ فعالیتهای ذهنی و فیزیکی ملایم نیز به حفظ ذخایر شناختی مغز کمک میکند.
درمان خانگی آنژیوپاتی آمیلوئید مغزی
استفاده از عبارت درمان خانگی برای بیماری پیچیده و خطرناکی که مستقیما با پاره شدن رگهای مغز در ارتباط است، باید با احتیاط فراوان همراه باشد. هیچ دارو، دمنوش گیاهی، یا روش سنتی در خانه وجود ندارد که بتواند رسوبات آمیلوئید را از داخل رگهای مغز شستشو داده یا از خونریزی رگهای آسیبدیده جلوگیری کند. تکیه بر ادعاهای غیرعلمی و درمانهای اینترنتی تاییدنشده، تنها باعث هدر رفتن زمان طلایی برای مدیریت صحیح پزشکی میشود و میتواند جان بیمار را به شدت به خطر بیندازد. درمان خانگی در اینجا فقط به معنای ایجاد یک محیط حمایتی و ایمن برای بهبود کیفیت زندگی بیمار است.
مراقبتهای خانگی باید بر محور پیشگیری از آسیبهای فیزیکی و کاهش استرسهای محیطی استوار باشد. از آنجا که بیماران به دلیل آسیبهای مغزی ممکن است دچار مشکلات تعادلی و گیجی باشند، خطر زمین خوردن در خانه بسیار بالاست. همانطور که گفته شد، ضربه به سر برای این رگهای شکننده یک فاجعه است. بنابراین چیدمان خانه باید تغییر کند؛ مسیرهای رفتوآمد باید از وسایل اضافی پاک شوند، لبههای تیز مبلمان پوشانده شوند و نور کافی در شبها فراهم گردد. استفاده از واکر یا عصا برای حفظ تعادل بیمار در خانه به شدت توصیه میشود.
از سوی دیگر، خانوادهها باید وظیفه نظارت دقیق بر مصرف داروها را بر عهده بگیرند. بیمار سالمندی که دچار اختلال حافظه شده است، ممکن است مصرف داروی فشار خون خود را فراموش کند یا آن را دو بار بخورد که هر دو حالت بسیار خطرناک است. تهیه جعبههای یادآور قرص و دادن داروها در زمان دقیق، یک اقدام خانگی بسیار موثر است. همچنین پرهیز کامل از دادن داروهای مسکن بدون نسخه مانند ایبوپروفن یا نوافن به بیمار بدون مشورت با پزشک ضروری است، زیرا این داروها میتوانند در روند انعقاد خون اختلال ایجاد کرده و خطر نشت خون در مغز را بالا ببرند. ایجاد محیطی آرام و به دور از تنشهای عصبی نیز به کنترل طبیعی فشار خون کمک شایانی میکند.
رژیم غذایی مناسب برای آنژیوپاتی آمیلوئید مغزی
اگرچه رژیم غذایی نمیتواند بیماری عروق آمیلوئیدی را درمان کند، اما تغذیه صحیح یک ابزار قدرتمند برای حمایت از سلامت عمومی رگهای خونی، کنترل فشار خون و کاهش التهاب سیستمیک در بدن است. غذایی که مصرف میکنیم میتواند به عنوان یک سپر محافظ برای سلولهای عصبی عمل کرده یا برعکس، روند فرسایش آنها را تسریع نماید. بهترین و علمیترین الگوی تغذیهای که برای حفظ سلامت مغز و عروق در سالمندان پیشنهاد میشود، ترکیبی از رژیم غذایی مدیترانهای و رژیم دش (DASH) است که در مجموع به آن رژیم غذایی مایند (MIND Diet) میگویند.
در این الگوی تغذیهای، محوریت با مواد غذایی گیاهی و کاهش شدید چربیهای حیوانی و قندهای تصفیه شده است. مصرف روزانه سبزیجات با برگهای سبز تیره (مانند اسفناج، کاهو و کلم بروکلی) که سرشار از آنتیاکسیدانها، ویتامینها و فولات هستند، به شدت توصیه میشود. این مواد به کاهش التهاب دیواره رگها کمک میکنند. میوههای رنگارنگ، به ویژه توتها (مانند بلوبری، توتفرنگی و شاهتوت) به دلیل داشتن مقادیر بالای فلاونوئیدها، محافظان قدرتمندی برای سلولهای مغزی در برابر استرس اکسیداتیو محسوب میشوند. مغزهای خام مانند گردو و بادام، روغن زیتون فرابکر و غلات کامل نیز از ارکان اصلی این رژیم هستند که چربیهای سالم و فیبر مورد نیاز بدن را تامین میکنند.
نکته بسیار حیاتی در رژیم غذایی این بیماران، محدودیت شدید و وسواسگونه در مصرف نمک (سدیم) است. نمک یکی از اصلیترین عوامل افزایش فشار خون است و افزایش فشار خون به معنای وارد آمدن فشار فیزیکی به رگهای شکننده مغز میباشد. مصرف غذاهای فرآوری شده، کنسروها، فستفودها و تنقلات شور باید به طور کامل متوقف شود و برای طعم دادن به غذاها از گیاهان معطر و آبلیموی تازه استفاده گردد. همچنین، مصرف ماهیهای چرب مانند سالمون که سرشار از اسیدهای چرب امگا-۳ هستند، حداقل دو بار در هفته برای حفظ انعطافپذیری نسبی عروق و سلامت قلب بسیار مفید است. پرهیز از مصرف گوشت قرمز پرچرب و کره حیوانی نیز به جلوگیری از تصلب شرایین و تنگتر شدن رگهای درگیر کمک میکند.
ارتباط آنژیوپاتی آمیلوئید مغزی با بیماری آلزایمر
یکی از جالبترین و در عین حال پیچیدهترین مباحث در علم عصبشناسی، ارتباط تنگاتنگ و خویشاوندی نزدیک بین این بیماری عروقی و بیماری آلزایمر است. وقتی محققان به بررسی ریشه این دو بیماری میپردازند، متوجه میشوند که هر دو آنها یک متهم اصلی و مشترک دارند: پروتئین بتا-آمیلوئید. این اشتراک پروتئینی باعث میشود که این دو اختلال مغزی در بسیاری از افراد سالمند به صورت همزمان رخ دهند و علائم یکدیگر را تشدید کنند.
تفاوت اصلی در اینجاست که در بیماری آلزایمر، پروتئینهای معیوب بتا-آمیلوئید در فضای بین سلولهای عصبی (نورونها) رسوب کرده و پلاکهایی را تشکیل میدهند که باعث اختلال در ارتباط بین سلولها و مرگ تدریجی آنها میشود. اما در بیماری آنژیوپاتی آمیلوئید، همان پروتئینها مسیر خود را به سمت دیواره رگهای خونی کج کرده و در آنجا انباشته میشوند. مطالعات کالبدشکافی نشان داده است که بیش از هشتاد درصد بیمارانی که با تشخیص قطعی آلزایمر از دنیا رفتهاند، درجات مختلفی از رسوب آمیلوئید در رگهای خونی مغز خود نیز داشتهاند. این یعنی مغز بیمار از دو جبهه تحت حمله قرار دارد: یکی تخریب مستقیم سلولها و دیگری اختلال در سیستم خونرسانی.
این همپوشانی باعث میشود که مرز بین علائم این دو بیماری بسیار باریک باشد. وقتی رگهای خونی نتوانند اکسیژن کافی را به بافت مغز برسانند (به دلیل رسوب در رگها)، روند زوال عقل و از دست دادن حافظه در بیمار آلزایمری با سرعت بسیار بیشتری پیش میرود. از سوی دیگر، بیماران مبتلا به آلزایمر که دچار ضعف عروقی آمیلوئیدی نیز هستند، به شدت در معرض خطر خونریزیهای مغزی قرار دارند، به خصوص اگر برای مشکلات قلبی خود داروهای رقیقکننده مصرف کنند. درک این ارتباط عمیق برای پزشکان بسیار مهم است، زیرا به آنها هشدار میدهد که هنگام درمان اختلال حافظه در یک فرد سالمند، حتما سلامت رگهای مغزی او را نیز از نظر خطر خونریزی بررسی کنند و در تجویز داروها بالاترین سطح احتیاط را به کار گیرند.
جمع بندی
بیماری آنژیوپاتی آمیلوئید مغزی (CAA) یک اختلال عروقی پیشرونده و مرتبط با افزایش سن است که در آن، تجمع غیرطبیعی پروتئین آمیلوئید در دیواره رگهای کوچک و متوسط مغز رخ میدهد. این رسوبات باعث میشوند رگهای خونی انعطافپذیری خود را از دست داده و به شدت شکننده شوند. نتیجه این فرآیند، ناتوانی رگها در تحمل فشار خون طبیعی و در نهایت بروز نشتهای میکروسکوپی یا خونریزی لوبار وسیع در سطح مغز است. این خونریزیها میتوانند علائم عصبی شدیدی مانند فلج ناگهانی، سردردهای کوبنده، افت شناختی و حتی مرگ را به دنبال داشته باشند.
تشخیص این بیماری چالشبرانگیز است و عمدتا با تکیه بر اسکنهای پیشرفته امآرآی و بررسی علائم بالینی بر اساس معیارهای بوستون صورت میگیرد. از آنجا که این عارضه پیوند سلولی و پروتئینی بسیار نزدیکی با بیماری آلزایمر دارد، بسیاری از بیماران همزمان علائم زوال عقل را نیز تجربه میکنند. تاکنون هیچ درمان قطعی برای پاکسازی این پروتئینها از رگهای مغز کشف نشده است؛ بنابراین مدیریت بیماری بر پایه کنترل سختگیرانه فشار خون و پرهیز جدی از مصرف داروهای رقیقکننده خون استوار است تا خطر پارگی رگها به حداقل برسد.
طول درمان این وضعیت مادامالعمر است و بیماران سالمند نیازمند مراقبتهای ویژه برای جلوگیری از سقوط و ضربه به سر هستند. با وجود اینکه پیشگیری قطعی از رسوب این پروتئینها امکانپذیر نیست، اما اصلاح سبک زندگی از طریق پیروی از رژیم غذایی مایند، محدودیت شدید نمک و ترک دخانیات میتواند به حفظ سلامت عمومی سیستم قلب و عروق کمک کرده و از سرعت پیشرفت آسیبها بکاهد. آگاهی از خطرات این بیماری پنهان و همکاری نزدیک با تیمی از متخصصان مغز و اعصاب، کلید حفظ کیفیت زندگی در دوران سالمندی است.

